En las células de mamíferos, tanto las células normales como las células malignas en proliferación necesitan obteneraminoácidos esenciales (EAA)para mantener las actividades de la vida normal. Los aminoácidos esenciales (metionina, valina, lisina, isoleucina, fenilalanina, leucina, treonina, histidina) no son solo proteínas, lípidos, ácidos nucleicos y otras macromoléculas biológicas La síntesis proporciona" materias primas" y también puede actuar como una molécula señal para inducir la activación de la vía mTOR.
En comparación con las células normales, las células tumorales a menudo muestran la característica importante de absorber una gran cantidad de aminoácidos esenciales. Sin embargo, el mecanismo molecular del metabolismo anormal de los aminoácidos esenciales aún no está claro.
El 26 de diciembre, el grupo de investigación del profesor Qing Guoliang del Instituto de Investigación Médica de la Universidad de Wuhan publicó resultados de investigación en línea titulados" El MYC oncogénico activa un bucle regulador de retroalimentación que promueve el metabolismo de aminoácidos esenciales y la tumorigénesis" en Informes de celda. La investigación informó sobre el bucle de retroalimentación positiva Myc -SLC7A5 / SLC43A1 reprograma el mecanismo molecular del metabolismo de los aminoácidos esenciales para promover el desarrollo maligno de tumores. Este estudio no solo revela un nuevo mecanismo por el cual las anomalías metabólicas promueven la tumorigénesis y el desarrollo, sino que también proporciona un objetivo potencial para el tratamiento de pacientes con tumores con alta expresión de MYC.
MYC es una proteína clave en la regulación del metabolismo tumoral. En este estudio, los investigadores demostraron por primera vez que la oncoproteína MYC es un regulador transcripcional clave que activa la absorción de aminoácidos esenciales por las células tumorales. Entonces, ¿cómo se regula MYC?
Muchos estudios en el pasado han demostrado que muchas proteínas miembros de la familia SLC (como SLC7A5 / A8, SLC43A1 / A2, SLC6A14, SLCA1-A11 y otros transportadores de aminoácidos) participan en la regulación de la ingesta de aminoácidos esenciales. Con la información anterior, es obvio preguntarse si MYC regula las proteínas de la familia SLC mencionadas anteriormente. Investigaciones posteriores encontraron que MYC regula la expresión de SLC7A5 y SLC43A1 a través de la activación directa y forma un bucle de retroalimentación positiva MYC-SLC7A5 / SLC43A1, que mejora la captación de aminoácidos esenciales por las células tumorales e inhibe la vía de estrés GCN2-eIF2α-ATF4. Luego activa selectivamente la traducción de proteínas de genes clave que promueven el cáncer como Myc, Bcl2, Cyclin D1 y, en última instancia, promueve el desarrollo maligno de tumores (abajo).
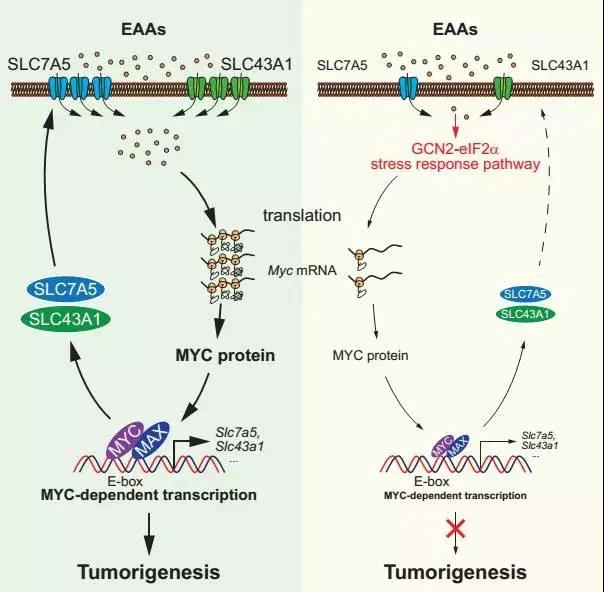
La activación continua de este bucle no solo asegura la ingesta de aminoácidos esenciales, sino que también conecta en cascada toda la red reguladora transcripcional mediada por Myc para promover la reprogramación metabólica de nutrientes clave como glucosa, glutamina, nucleótidos y ácidos grasos. Interferir con la función de SLC7A5 / SLC43A1 puede interrumpir este bucle de señal de retroalimentación positiva, hacer que la expresión de Myc, Bcl2 y Cyclin D1 disminuya en modelos tumorales in vivo e in vitro, e inducir selectivamente la apoptosis de células tumorales que sobreexpresan Myc. Los resultados anteriores sugieren que el anticuerpo monoclonal dirigido a SLC7A5 / SLC43A1 puede usarse como un tratamiento potencial para pacientes con tumores con alta expresión de MYC.
Se informa que el profesor Qing Guoliang y el profesor Liu Hudan del Instituto de Investigación Médica de la Universidad de Wuhan son los autores correspondientes del artículo, y el estudiante de doctorado Yue Ming es el primer autor del artículo.